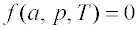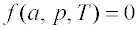adsorpce z plynné fáze na tuhé látce
adsorption at solid/gas interface
Děj, při němž jsou molekuly plynů vázány silovým polem tuhé látky k jejímu
povrchu. Jsou-li působící síly fyzikální povahy jedná se o nespecifickou
fyzikální adsorpci, která probíhá na celém povrchu tuhé látky. Vzniká-li mezi adsorbovanou molekulou a povrchem chemická vazba, je děj označován jako
chemisorpce, která je velmi specifická.
Kvantitativní charakteristikou adsorpce plynů na tuhých látkách je množství plynu, vyjádřené v molech jako hmotnost (obvyklé označení a), či objem υ, přepočtený na normální podmínky, které je naadsorbované na jednotce hmotnosti pevné látky. Adsorbované množství je závislé jak na povaze adsorbujícího se plynu, tak na povaze tuhé látky, na velikosti povrchu, na parciálním tlaku adsorbující se složky v plynné fázi a na teplotě.
Experimentální stanovení adsorpce z plynné fáze na pevných adsorbentech je poměrně náročné. Nejčastěji se měří adsorbované množství v závislosti na rovnovážném tlaku plynu při konstantní teplotě (viz
měření adsorpce z plynné fáze) nebo změna adsorbovaného množství s teplotou při konstantním rovnovážném tlaku plynu. Adsorbované množství se stanovuje ze změn tlaku plynu v určitém objemu -
volumetrické metody) nebo ze změny váhy adsorbentu -
gravimetrické metody ve statických nebo průtokových aparaturách.
Adsorpce je charakterizována vzájemnou závislostí adsorbovaného množství, teploty a rovnovážného tlaku adsorbujícího se plynu:
Nejčastěji jsou měřeny
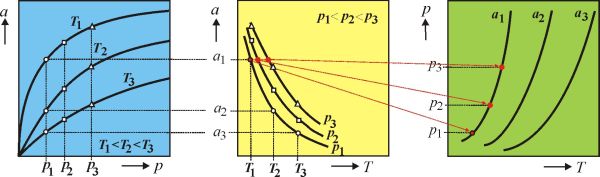
adsorpční izotermy (obr. 1); při konstantní teplotě se měří rovnovážný tlak plynu a adsorbované množství. Rovněž se experimentálně stanovují
adsorpční izobary, tj. změna adsorbovaného množství s teplotou při konstantním rovnovážném tlaku plynu, které je možno také sestrojit z izoterem naměřených při různých teplotách (obr. 2). Z těchto závislostí se konstruují
adsorpční izostery (obr. 3), tj. závislosti rovnovážného tlaku plynu na teplotě při konstantním adsorbovaném množství, které jsou užitečné pro výpočet
adsorpčních tepel.
|
Obr. 1 Adsorpční
izotermy, a = a(p); [T]
|
Obr. 2 Adsorpční
izobary, a = a(T); [p]
|
Obr. 3 Adsorpční
izostery, p = p(T); [a]
|
Ke zpracování experimentálních dat a jejich případné interpolace či extrapolace je vhodné mít k dispozici analytické vyjádření závislosti mezi rovnovážným adsorbovaným množstvím plynu a jeho tlakem. Nejstarším, dosud používaným analytickým vyjádřením závislosti adsorbovaného množství na rovnovážném tlaku za konstantní teploty je
Freundlichova izoterma. Pro monovrstvou adsorpci byla na základě kinetických představ odvozena
Langmuirova izoterma.
Adsorpční izoterma BET je rozšířením Langmuirovy izotermy na vícevrstvou adsorpci. Jiný způsobem zpracovává problém vícevrstvé adsorpce
Polányho potenciální teorie. Upravené rovnice pro adsorpci čistých plynů se používají také pro popis
adsorpce ze směsí plynů.
U pórovitých adsorbentů se za vyšších tlaků na velikosti adsorbovaného množství vedle fyzikální adsorpce podílí ještě další proces,
kapilární kondenzace.
Adsorpce je vždy děj exotermní; adsorbované množství při konstantním tlaku tedy s rostoucí teplotou vždy klesá.
Adsorpční tepla se stanovují experimentálně v kalorimetrech nebo se určují z adsorpčních izoster. Hodnoty adsorpčních tepel pro chemisorpci jsou řádově vyšší než pro fyzikální adsorpci.
Kinetika adsorpce byla studována hlavně v souvislosti s problematikou plynných reakcí katalyzovaných tuhými katalyzátory.
Grafy souvislostí do úrovně:
I  II
II